オゾンの構造式 102回薬剤師国家試験問9の解説
102回薬剤師国家試験 問9
オゾン(O3)の構造式として最もふさわしいのはどれか。1つ選びなさい。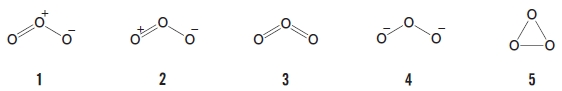
102回薬剤師国家試験 問9 解答解説
の構造式として最もふさわしいのはどれか.jpg)
この構造は、全原子がオクテット則を満たし、安定であるため、
オゾン(O3)の構造式として最もふさわしいと考えられます。
以下で詳細を解説します。
酸素原子の価電子数は6個です。
オゾンの価電子数は、
酸素 6個 × 3原子 = 18個
です。
価電子数から全原子がオクテット則を満たすことを考えて構造を描くと、
下記のようになります。

この構造の価電子数は、
二重結合の電子4個 + 単結合の電子2個 + 非共有電子対12個 = 18個
ですので、先ほど計算した数と合っています。
この構造における各酸素のまわりの電子数は次のようになります。

全原子の周囲の電子数が8個であるので、
全原子がオクテット則を満たし、安定になっています。
以上より、
オゾンの構造式として最もふさわしいのは、
選択肢1だと考えられます。
なお、オゾンは下記のように共鳴していると考えられます。
