亜鉛がとりやすい酸化数 103回薬剤師国家試験問9の解説
103回薬剤師国家試験 問9
亜鉛イオンは、生体内においてルイス酸として重要な役割を果たしている。
亜鉛がとりやすい酸化数はどれか。1つ選びなさい。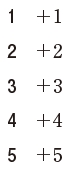
103回薬剤師国家試験 問9 解答解説
亜鉛がとりやすい酸化数は+2である。

亜鉛(Zn)は、原子番号30の元素で、電子配置は次のように表されます。
Zn:1s2 2s2 2p6 3s2 3p6 3d10 4s2
亜鉛がイオンになるときは、
最外殻にある 4s電子2個 を失いやすいため、通常は
Zn → Zn2+ + 2e−
となります。
以下で亜鉛がイオンになるときZn2+になりやすい理由を説明します。
Zn2+の電子配置と安定性
Zn2+の電子配置は次のように表されます。
Zn2+:1s2 2s2 2p6 3s2 3p6 3d10
この 3d10 はd軌道が完全に満たされた安定な電子配置です。
Zn+の場合
Zn+は、4s電子を1個だけ失った状態です。
その電子配置は次のように表されます。
Zn+:1s2 2s2 2p6 3s2 3p6 3d10 4s1
Zn+は4s軌道に電子が1個残っており、Zn2+ほど安定ではありません。
Zn3+の場合
Zn3+になるには、4s電子2個を失った後、さらに3d電子を1個失う必要があります。
その電子配置は次のように表されます。
Zn3+:1s2 2s2 2p6 3s2 3p6 3d9
しかし、これは安定な 3d10 を崩すことになります。
そのため、Zn3+はZn2+ほど安定ではありません。
Zn4+やZn5+も同様にZn2+ほど安定ではありません。
以上より、
亜鉛は+2の酸化数をとりやすいです。
生体内でのZn2+とのつながり
生体内で重要なのは、亜鉛が多くの場合 Zn2+ として存在し、
酵素の活性中心などで働くことです。
Zn2+ は、電子対を受け取る性質があるため、ルイス酸として働きます。
周囲の分子の酸素原子や窒素原子などから電子対を受け取って配位結合をつくります。
酵素の活性中心で水分子や基質と相互作用し、反応を進みやすくする役割を担います。
亜鉛が生体内でルイス酸として機能する例として、
金属プロテアーゼの活性中心に存在する亜鉛イオンに水分子が配位することで、
水分子の電子密度が低下してO−H結合が切れやすくなって水分子が活性化し、
タンパク質やペプチドの結合の加水分解を起こりやすくなることがあります。